✦ Het essentiële in 30 seconden
Toen KJ Muldoon in 2024 werd geboren, had hij een ultra-zeldzame genetische aandoening die de helft van de aangedane baby's in de eerste weken doodt. In 2025 deed een Amerikaans team iets ongekends: in zes maanden ontwierpen zij een CRISPR-behandeling op maat voor dit ene kind. Vandaag gaat het goed met KJ — en de geneeskunde heeft een drempel overschreden.
Eén baby, één medicijn, zes maanden
Toen hij in augustus 2024 werd geboren, had KJ Muldoon weinig kans om lang te leven. Hij kwam ter wereld met een genetische ziekte die ongeveer één op 1,3 miljoen mensen wereldwijd treft: CPS1-deficiëntie. Eén verkeerd gespelde letter in zijn DNA belet zijn lever om ammoniak af te voeren — een afvalstof die ontstaat wanneer ons lichaam eiwitten verteert.
Zonder behandeling stapelt ammoniak zich op, raakt de hersenen beschadigd, en sterft de helft van de baby's met de ernstige vorm in de eerste weken. Conventionele opties zijn slecht: een streng eiwitarm dieet geeft enkele maanden overleving, een levertransplantatie is pas mogelijk na meerdere maanden leven.
In het Children's Hospital of Philadelphia deed een team iets ongekends. In zes maanden ontwierpen, produceerden en dienden ze een medicijn toe op maat gemaakt voor hem alleen. Dat medicijn is CRISPR.
Wat is CRISPR?
Stel je DNA voor als een gigantisch kookboek — drie miljard letters die je lichaam vertellen hoe het zich moet opbouwen. Wanneer één letter verkeerd is, zoals een typfout in het recept, kan het hele gerecht mislukken.
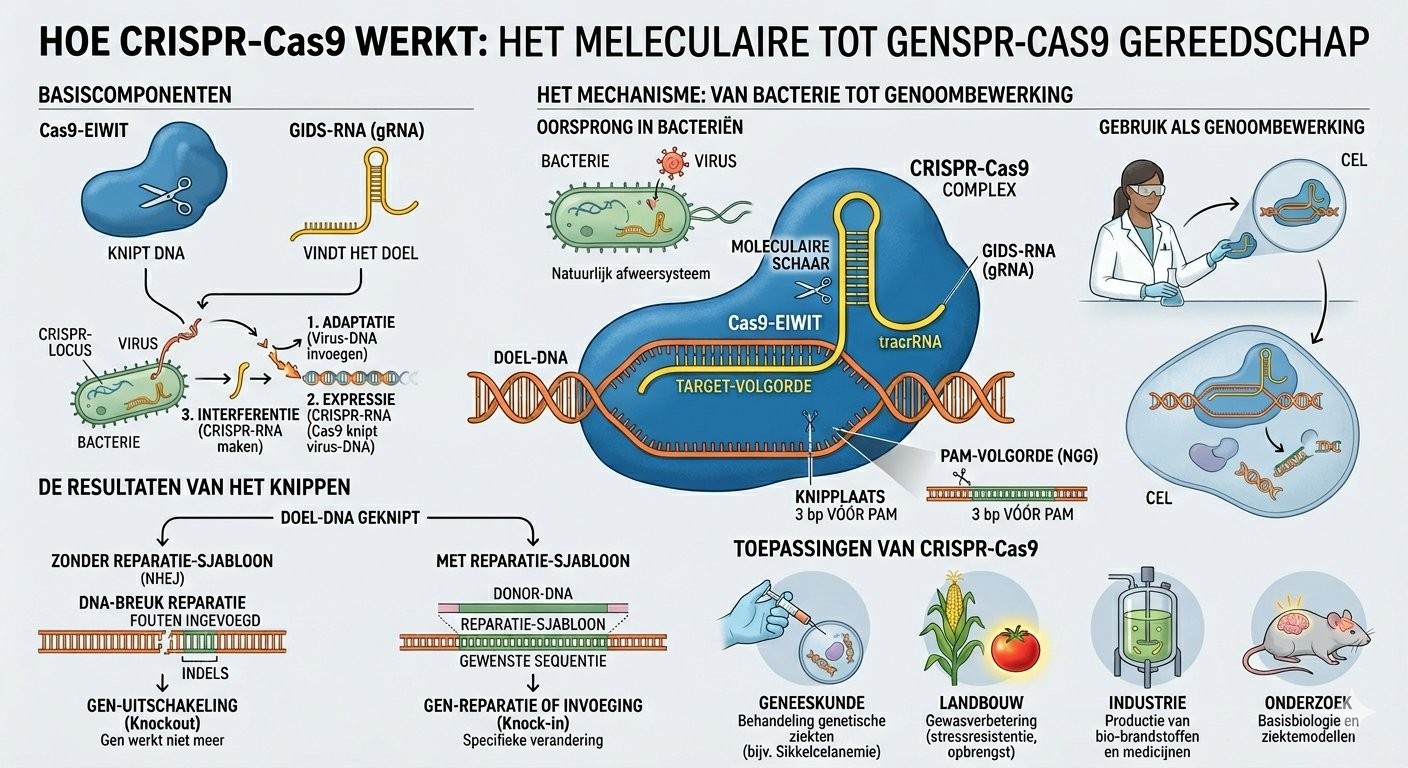
CRISPR is een moleculaire schaar met ingebouwde GPS. De GPS is een klein stukje RNA (de chemische neef van DNA) dat het recept kan lezen en precies die zin vindt die moet worden gecorrigeerd. Eenmaal ter plaatse knipt een eiwit genaamd Cas9. De cel zorgt dan voor de reparatie — en als ze goed wordt begeleid, kan ze repareren met de juiste letter.
Deze technologie bestaat sinds 2012. Ze leverde Emmanuelle Charpentier en Jennifer Doudna de Nobelprijs voor Scheikunde 2020 op. Wat in 2025 veranderde met de casus van baby KJ, is dat ze voor het eerst werd gebruikt om één enkele unieke patiënt ter wereld te behandelen.
Waarom dit een historische wending is
Tot nu toe werden medicijnen ontworpen voor miljoenen mensen. Een nieuwe behandeling ontwikkelen duurt tien jaar en kost ongeveer een miljard. Voor ultra-zeldzame ziekten — die slechts een handvol individuen wereldwijd treffen — heeft geen enkel farmaceutisch bedrijf een economische reden om iets te ontwikkelen.
De casus KJ bewijst dat het veel sneller kan. En dat de toekomst van de geneeskunde misschien niet meer één medicijn voor iedereen is, maar een medicijn voor elk individu.
🔍 Om te onthouden
- →KJ Muldoon is de eerste mens behandeld met een CRISPR-therapie specifiek voor hem ontworpen
- →Zijn ziekte (CPS1-deficiëntie) treft 1 op de 1,3 miljoen mensen — geen enkel lab zou een specifiek medicijn ontwikkelen
- →De behandeling werd ontworpen, vervaardigd en toegediend in 6 maanden — tegenover 10 jaar gewoonlijk
- →KJ werd in juni 2025 uit het ziekenhuis ontslagen en groeit vandaag normaal op
✦ Tot besluit
De toekomst van de geneeskunde wordt misschien patiënt per patiënt geschreven.
The baby went home on June 3, 2025, after 307 days in hospital. He eats more protein than before. He needs fewer medications. He's growing. What the KJ case tells us isn't just a beautiful medical story — it's proof that genetics has crossed a threshold. Until now, rare diseases were orphans: too few patients to interest the labs. With this demonstration, the question is no longer whether we can tailor treatment, but how long and how much money it will take to make it accessible to other children.
✦ Gratis nieuwsbrief
Het volgende artikel
rechtstreeks in je mailbox?
Gratis · Geen spam · Om de twee weken.
✦ Samenvatting (gemiddeld niveau)
KJ Muldoon, born in 2024 with an ultra-rare CPS1 deficiency (a urea-cycle enzyme), became in 2025 the first patient treated with a fully personalized CRISPR therapy. The team led by Musunuru and Ahrens-Nicklas in Philadelphia used base editing — a more precise evolution of classical CRISPR-Cas9 — to correct KJ's specific mutation. From design to infusion: 6 months. Published in the NEJM in May 2025.
CRISPR-Cas9: van bacteriële afweer tot klinische geneeskunde
CRISPR werd niet uitgevonden. Het werd geleend. Miljoenen jaren lang gebruikten bacteriën het om zich te verdedigen tegen virussen. Bij een virale aanval bewaren sommige bacteriën een stukje van het virale DNA in een zone van hun genoom genaamd CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats). Als het virus terugkomt, vindt en knipt een eiwit genaamd Cas9, geleid door een RNA-kopie van dat fragment, het in twee.
In 2012 publiceerden Emmanuelle Charpentier en Jennifer Doudna in Science een artikel dat alles veranderde: ze toonden aan dat dit systeem herprogrammeerd kan worden door het gids-RNA te vervangen door eender welke sequentie. Sindsdien is CRISPR-Cas9 niet langer een bacterieel afweermechanisme — het is een universeel genoombewerkingsinstrument, toepasbaar op elke levende cel.
December 2023: het eerste goedgekeurde CRISPR-medicijn
Thirteen years after the foundational paper, the US FDA and the UK's UKMHRA approved Casgevy (exa-cel), developed by Vertex Pharmaceuticals and CRISPR Therapeutics. This treatment addresses sickle cell disease and beta-thalassemia.
Het principe: men neemt de stamcellen van de patiënt af, bewerkt ze buiten het lichaam (ex vivo) om een gen dat sinds de kindertijd inactief is opnieuw te activeren (het foetale hemoglobinegen), en geeft ze daarna terug. Resultaat bij behandelde patiënten: de pijnlijke crises die kenmerkend zijn voor sikkelcelziekte verdwijnen.
Maar Casgevy blijft een "massa"-behandeling: hetzelfde protocol voor elke patiënt. De casus KJ introduceert iets anders.
Baby KJ: N-of-1-geneeskunde
KJ Muldoon werd geboren in augustus 2024. Enkele dagen na zijn geboorte overschrijdt zijn ammoniakgehalte in het bloed de 1000 µmol/L — het normale bereik ligt tussen 9 en 33. De diagnose: ernstige deficiëntie van carbamoylfosfaatsynthetase 1 (CPS1), een leverenzym van de ureumcyclus. Zonder dit enzym kan ammoniak niet in ureum worden omgezet en uitgescheiden. Het stapelt zich op. Het valt de hersenen aan.
Kiran Musunuru (University of Pennsylvania) and Rebecca Ahrens-Nicklas (Children's Hospital of Philadelphia) decided to try something else. They identified the two specific mutations in KJ's CPS1 gene, then designed a therapy tailored to those mutations. The whole thing took six months from design to infusion.
De sleutel: ze gebruikten geen klassieke CRISPR-Cas9. Ze gebruikten een recentere en preciezere evolutie: base editing.
Base editing: CRISPR met hogere resolutie
Classical CRISPR creates double-strand breaks in DNA. It's effective but risky: the cell may repair incorrectly, sometimes creating major chromosomal rearrangements.
Base editing knipt niet. Het zet chemisch één DNA-letter om in een andere — bijvoorbeeld een A in een G — rechtstreeks ter plaatse, zonder breuk. Voor de casus KJ ontwierp het team een bewerking die één van de twee mutaties die verantwoordelijk zijn voor zijn deficiëntie corrigeert, net genoeg om een minimaal niveau van functioneel enzym te herstellen.
De behandeling werd via lipide-nanodeeltjes aan de lever afgeleverd (dezelfde technologie als de mRNA-COVID-vaccins). Drie doses, tussen februari en april 2025.
Vandaag: wat we weten, wat we niet weten
Wat we weten: KJ werd 307 dagen na zijn opname ontslagen. Hij kan meer eiwitten eten dan voorheen. Hij heeft minder ammoniak-verlagende medicijnen nodig. Hij groeit normaal op.
Wat we niet weten: hoe lang het effect zal duren, of de bewerking behouden blijft naarmate zijn levercellen zich vernieuwen, en of in de komende jaren off-target-effecten aan het licht zullen komen.
🔍 Belangrijke punten
- →CRISPR-Cas9 = herprogrammeerd bacterieel immuunsysteem als universeel bewerkingsinstrument (Jinek et al., Science 2012)
- →Casgevy (december 2023): eerste goedgekeurde CRISPR-medicijn, voor sikkelcelziekte en β-thalassemie — ex vivo-aanpak, zelfde protocol voor iedereen
- →Casus KJ (februari 2025): eerste "N-of-1" CRISPR-therapie — in vivo base editing via lipide-nanodeeltjes, gericht op één unieke mutatie
- →Historische tijdscompressie: 6 maanden van ontwerp tot infusie, tegenover ~10 jaar voor een klassiek medicijn
✦ Tot besluit
Prototype van een model, geen geïsoleerde uitzondering.
According to the Innovative Genomics Institute, roughly 250 clinical trials worldwide are currently using genome-editing tools, more than 150 of them active. Most are still testing uniform protocols for patient groups. But two US programs launched in 2025 (ARPA-H's THRIVE and GIVE) aim explicitly to make the "N-of-1" approach replicable: to build the regulatory and industrial infrastructure needed to compress 10 years of development into 6 months for any child with an ultra-rare mutation. If it works, it's a paradigm shift. If it doesn't, KJ will remain a magnificent but isolated exception. The next three years will decide.
✦ Uitgebreide samenvatting
Musunuru, Ahrens-Nicklas et al. (NEJM, 2025) rapporteren het eerste klinische geval van een gepersonaliseerde N-of-1 genoombewerkingstherapie bij een zuigeling met ernstige carbamoylfosfaatsynthetase 1-deficiëntie (CPS1). Het team ontwierp een adenine-base-editor (ABE) gericht op de specifieke trunceringvarianten van de patiënt, afgeleverd via lipide-nanodeeltjes in drie systemische doses (februari–april 2025). De pipeline — van mutatie-identificatie tot infusie — werd afgerond in ~6 maanden. De patiënt verdraagt meer eiwitinname, heeft minder ammoniak-scavengers nodig, en werd na 307 dagen hospitalisatie ontslagen.
Moleculaire architectuur van de KJ-behandeling
De therapie die aan KJ werd toegediend, is geen conventionele CRISPR-Cas9. Het is een adenine-base-editor (ABE), een van CRISPR afgeleide architectuur die fundamenteel verschilt in zijn werkingsmechanisme.
Een ABE bestaat uit drie gefuseerde modules:
- Een Cas9-"nickase" (nCas9), waarbij één van de twee nuclease-activiteiten (HNH) is uitgeschakeld door een puntmutatie. Ze snijdt slechts één DNA-streng in plaats van twee — waardoor de dubbelstrengsbreuk wordt vermeden.
- Een geëvolueerd adenine-deaminase (ABE8e), dat chemisch een adenine (A) omzet in inosine (I, door het cellulaire apparaat gelezen als guanine G).
- Een gids-RNA van 20 nucleotiden, complementair aan de doelwitsequentie, naast een PAM (NGG-motief voor Cas9 van Streptococcus pyogenes).
Concreet: het doelwit wordt gelokaliseerd via RNA-DNA-paring, één streng wordt ingesneden, en het deaminase wijzigt chemisch een specifieke A binnen een bewerkingsvenster van ongeveer 4–8 nucleotiden. Na replicatie wordt de tegenoverliggende streng gekopieerd van de gewijzigde streng, waardoor de A→G-mutatie permanent wordt vastgelegd.
In KJ's case, the Musunuru team specifically targeted the truncating mutations in the CPS1 gene and designed a guide RNA enabling an A→G conversion restoring correct reading of the relevant exon. The NEJM publication (DOI: 10.1056/NEJMoa2504747) beschrijft het ontwerp en de snelle preklinische tests in gehumaniseerde muizen vóór toediening aan de patiënt.
Waarom base editing het speelveld verandert
Het cruciale verschil tussen klassieke CRISPR-Cas9 en base editing ligt in het veiligheidsprofiel. Grote deleties en chromosomale herschikkingen komen bij base editors ongeveer 20 keer minder vaak voor dan bij klassieke Cas9-nucleasen.
Dat is essentieel, want de grootste risico's van conventionele CRISPR-Cas9 zijn niet alleen kleine inserties-deleties (indels) op off-target-sites, maar ook bredere structurele variaties: deleties van meerdere megabasen, chromosomale translocaties, en complexe herschikkingen op de bewerkingssite zelf.
Voor een zuigeling van 7 maanden gaf de risico/baten-afweging duidelijk de voorkeur aan de technisch meest conservatieve aanpak, ook al richtte die zich op een "mindere" correctie (gedeeltelijk herstel van activiteit in plaats van volledige correctie).
Aflevering: de beperkende factor
KJ's therapy was delivered via lipid nanoparticles (LNPs) — the same platform as SARS-CoV-2 mRNA vaccines. LNPs encapsulate the mRNA coding the base editor and the guide RNA, and accumulate preferentially in the liver after IV administration, which is ideal when the target (here, CPS1-expressing hepatocytes) is hepatic.
Maar dat is ook een structurele beperking van het model. Levertropische LNP's werken goed voor de lever — vandaar de groei van studies op leverziekten (hATTR met Intellia's NTLA-2001, AATD-1, GSD1a met Beam Therapeutics). Voor andere weefsels (hersenen, spier, netvlies) zijn andere vectoren nodig: vooral AAV, met uitdagingen op het vlak van immunogeniciteit en cargocapaciteit (AAV's halen ongeveer 4,7 kb, wat krap is voor een volledige base editor).
Het wereldwijde klinische landschap in 2026
Volgens het Innovative Genomics Institute (update 2026) gebruiken ongeveer 250 klinische studies wereldwijd genoombewerking (CRISPR-Cas, base editing, prime editing, ZFN, TALEN), waarvan meer dan 150 actief. De belangrijkste therapeutische gebieden:
- Hemoglobinopathieën: Casgevy goedgekeurd (sikkelcelziekte, β-thalassemie); pediatrische uitbreidingen lopen.
- hATTR-amyloïdose: NTLA-2001 (Intellia) in fase 3, eerste CRISPR-therapie systemisch in vivo afgeleverd.
- Erfelijk angio-oedeem: NTLA-2002 (Intellia), fase 3.
- Rare metabolic diseases: N-of-1 approach from CHOP/Penn, Beam's programs (hATTR, GSD1a, AATD-1).
- Oncologie: CAR-T-studies verrijkt met bewerking (KO van PD-1, TRAC, enz.) — grotendeels fase 1/2.
De casus KJ is dus geen geïsoleerde uitzondering. Ze past in een bredere verschuiving van het klinische paradigma: van "platform"-therapieën (Casgevy) naar "bespoke"-therapieën (N-of-1). De Amerikaanse ARPA-H lanceerde in 2025 twee programma's (THRIVE en GIVE) specifiek om de reglementaire en productie-infrastructuur op te bouwen die nodig is om de KJ-aanpak voor andere patiënten te repliceren.
🔬 Beperkingen & vooruitzichten
- →Duurzaamheid van de bewerking: hepatocyten vernieuwen zich. Als de bewerking slechts een fractie van de hepatische stamcellen heeft bereikt, kan het therapeutische effect afnemen. Langetermijnopvolging is cruciaal.
- →Mozaïcisme: niet alle hepatocyten zijn bewerkt. De exacte bewerkingsratio werd nog niet in detail gepubliceerd — een gedeeltelijke correctie volstond om een leefbare metabole functie te herstellen.
- →sgRNA-onafhankelijke off-target-effecten: ABE8e-base editors vertonen een potentieel problematisch RNA-bewerkingsprofiel. De pediatrische opvolging moet transcriptomische monitoring omvatten.
- →Economische schaalbaarheid: behandelingskost in miljoenen USD, gedekt door CHOP en filantropische partners. Er bestaat geen terugbetalingsmodel voor N-of-1-therapieën — de echte bottleneck.
- →Reglementair kader: de FDA autoriseerde de behandeling onder een uitzonderlijk onderzoeksprotocol. Duurzame trajecten voor N-of-1-therapieën creëren is de uitdaging voor 2026–2028.
✦ Tot besluit
The real leap is not technological — it's organizational.
CRISPR is niet "de geneeskunde van de toekomst". Het is de geneeskunde van vandaag — maar niet in de zin die de meeste mensen denken. De publieke verbeelding blijft gefixeerd op "genetisch gemodificeerde baby's" (de He Jiankui-episode, 2018) of fantasieën over genetische verbetering. De klinische realiteit is prozaïscher en radicaler: CRISPR heeft al levens gered bij patiënten met sikkelcelziekte, en het heeft zojuist bewezen dat het in zes maanden kan worden ingezet om een unieke baby ter wereld te redden. Het team toonde aan dat met nauwe coördinatie tussen laboratorium, LNP-fabrikanten, CRO's en regelgevers, een proces dat doorgaans een decennium in beslag neemt, kan worden samengeperst in 180 dagen. Als deze keten repliceerbaar wordt, zal het de behandeling van ultra-zeldzame ziekten transformeren. De vraag is niet langer technisch. Ze is economisch, reglementair en organisatorisch.
Primaire bron
Musunuru K, Ahrens-Nicklas R, et al. Patient-Specific In Vivo Gene Editing to Treat a Rare Genetic Disease. New England Journal of Medicine. 2025. doi:10.1056/NEJMoa2504747. Project led by Children's Hospital of Philadelphia and Penn Medicine with philanthropic partners.
Belangrijkste referenties
-
[1]
Jinek M, Chylinski K, Fonfara I, Hauer M, Doudna JA, Charpentier E. A programmable dual-RNA–guided DNA endonuclease in adaptive bacterial immunity. Science. 2012;337(6096):816-821. doi:10.1126/science.1225829 — Baanbrekende paper over programmeerbare CRISPR-Cas9.
-
[2]
Innovative Genomics Institute. CRISPR Clinical Trials: A 2026 Update. April 2026. innovativegenomics.org/news/crispr-clinical-trials-2026 ↗ — Huidige stand van zaken in het klinische landschap.